Informasi Uji Klinik Vaksin COVID-19 Indovac Primer Anak
| Melalui informasi ini, kami bermaksud untuk mengajak anak Anda untuk ikut serta dalam penelitian yang akan kami lakukan. Keikutsertaan anak Anda sangat kami hargai dan bersifat sukarela. Anak Anda bisa memutuskan untuk keluar dari penelitian ini setiap saat. |
| Latar Belakang Penelitian |
| COVID-19 adalah penyakit menular yang disebabkan oleh jenis coronavirus yang baru ditemukan pada Desember 2019 yaitu virus SARS-CoV-2. Badan Kesehatan Dunia kemudian mengumumkan bahwa COVID-19 sebagai penyakit pandemi (penyakit wabah di seluruh negara) pada 11 Maret 2020. Bio Farma juga berperan dalam pengembangan vaksin SARS-CoV-2 yaitu dari jenis subunit protein rekombinan dengan menggunakan adjuvan berupa Alum dan CpG 1018. Adjuvan merupakan zat tambahan dalam vaksin yang berfungsi meningkatkan khasiat dari vaksin yang dikembangkan. |
| Kasus COVID-19 pada anak di Indonesia terus meningkat, dan mengalami tren kenaikan yang cukup tajam. Vaksinasi COVID-19 tidak hanya penting untuk usia dewasa tetapi juga pada anak, untuk dapat mencegah dan memutus rantai penularan COVID-19. |
| Tujuan Penelitian |
| Penelitian ini bertujuan untuk menilai keamanan dan kekebalan dari produk yang diteliti setelah pemberian dua dosis vaksin SARS-CoV-2 (protein subunit rekombinan dengan adjuvan alum + CpG 1018) atau kita sebut dengan Vaksin COVID-19 CpG Bio Farma atau Vaksin COVID-19 BUMN atau dikenal dengan Vaksin Indovac. |
| Peserta Penelitian |
| Peserta penelitian akan diambil sebanyak 1050 orang anak (usia 12-17 tahun), dengan rincian 1000 anak untuk evaluasi keamanan dan titer antibodi, serta 50 anak untuk evaluasi keamanan, titer antibodi, dan respon imun seluler. Anak-anak sehat usia 12-17 tahun. Peserta dan orang tua/wali peserta menerima penjelasan dan menandatangani Surat Persetujuan setelah Penjelasan (informed consent dan assent), dan menyetujui mengikuti aturan dan jadwal uji klinis. Anda/Anak Anda tidak bisa mengikut uji klnik ini jika memenuhi salah satu kriteria berikut: 1. Telah atau akan diikutsertakan dalam uji klinis lain. 2. Memiliki riwayat vaksinasi COVID-19 (berdasarkan wawancara). 3. Memiliki riwayat sakit COVID-19 dalam 3 bulan terakhir. 4. Menderita sakit ringan, sedang atau berat dan atau penyakit kronik dan demam (suhu aksila ≥ 37,5oC) yang diukur dengan thermometer sinar merah atau thermometer tembak. 5. Riwayat asma, alergi terhadap salah satu komponen vaksin (berdasarkan pemeriksaan). 6. Riwayat gangguan pembekuan darah atau penyakit darah lainnya yang merupakan kontraindikasi suntikan pada otot dalam. 7. Riwayat penyakit serius seperti masalah jantung, tekanan darah tinggi dan diabetes, penyakit hati dan ginjal, hingga kanker. 8. Subjek sedang terapi obat yang menyebabkan penurunan sistem imun dalam 4 minggu terakhir (immunoglobulin intravena, penggunaan produk darah atau kortikoterapi jangka panjang dan imunosupresan lainnya). 9. Riwayat kejang tidak terkontrol atau masalah syaraf lainnya seperti Gullain-Barre Syndrome. 10. Mendapat imunisasi apapun dalam waktu 4 minggu ke belakang atau akan menerima vaksin lain dalam waktu 4 minggu ke depan. 11. Peserta perempuan yang hamil atau berencana hamil selama periode penelitian (berdasarkan wawancara dan hasil tes urin kehamilan). 12. Subyek berencana pindah dari wilayah studi sebelum masa penelitian berakhir. |
| Lembaga yang Mendukung Penelitian |
| Penelitian in dilaksanakan oleh 3 center: Pusat Kajian Kesehatan Anak (PKKA-PRO), Universitas Gadjah Mada (UGM), Yogyakarta, Departemen Kesehatan Anak Fakultas Kedokteran Universitas Indonesia / RSUP dr. Cipto Mangunkusumo, Jakarta, dan Fakultas Kedokteran Universitas Andalas. Penelitian ini disponsori oleh PT Bio Farma, Badan Usaha Milik Negara (BUMN) yang memproduksi vaksin uji yang berlokasi di Bandung, Indonesia. |
| Prosedur Penilitan |
Anak Anda akan ikut serta dalam penelitian ini selama kurang lebih 12 bulan. Setelah anak Anda dinyatakan dapat berpartisipasi dalam penelitian, akan dilakukan prosedur pengacakan untuk menentukan apakah anak Anda akan mendapatkan Vaksin Uji (COVID-19 CpG Bio Farma) atau Vaksin Pembanding (vaksin COVID-19 yang sudah ada di pasaran). Dokter Penelitian maupun anak Anda tidak mengetahui vaksin yang diperoleh apakah vaksin COVID-19 CpG Bio Farma atau vaksin pembanding. Selama mengikuti penelitian, anak Anda akan melakukan kunjungan penelitian sesuai dengan jadwal penelitian, termasuk dua (2) kali kunjungan pemberian vaksin dan lima (5) kali pengumpulan sampel darah. Rincian jadwal penelitian disajikan dalam tabel dibawah ini: 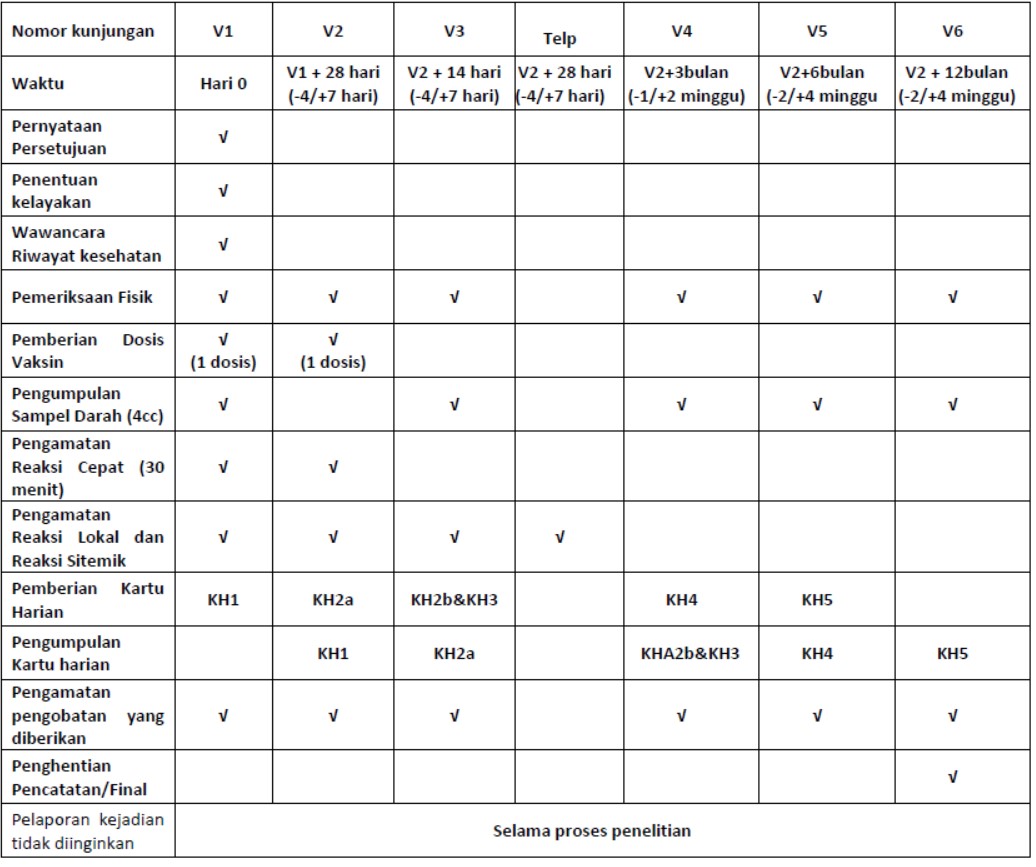 |
| Tanggung Jawab Anda Selama dalam Penelitian |
| Terdapat obat-obatan tertentu yang tidak boleh anak Anda konsumsi selama berpartisipasi dalam penelitian. Obat-obatan tersebut mencakup: Obat-obatan yang dapat mempengaruhi sistem kekebalan tubuh seperti pemberian terapi steroid di atas dosis tertentu.Obat/jamu penghilang nyeri atau penurun panas, yang dapat menyamarkan pengamatan keamanan vaksin.Immunoglobulin (antibody) atau produk bagi darah lainnya.Produk-produk penelitian lain. Jika anak Anda perlu mengkonsumsi obat-obatan ini, maka anak Anda menghubungi petugas penelitian sesegera mungkin. |
| Manfaat Keikutsertaan dalam Penelitian dan Kompensasi |
| Peserta dalam penelitian ini akan mendapat manfaat kekebalan terhadap penyakit COVID-19.Kesehatan dan kondisi anak Anda akan dipantau oleh petugas penelitian secara teratur selama jalannya penelitian ( hingga 12 bulan setelah pemberian dosis ke-2).Keikutsertaan anak Anda dalam penelitian ini, termasuk pemeriksaan darah tidak akan dikenai biaya apapun.Vaksin akan diberikan cuma-cuma.Biaya pengobatan bila peserta menderita sakit atau mengalami Kejadian Ikutan Pasca Imunisasi (KIPI) pada periode pemantauan keamanan (hingga 1 bulan setelah imunisasi terakhir) akan dibayarkan.Biaya transport dan kompensasi waktu akan untuk setiap kunjungan.Selama kunjungan penelitian terjadwal di fasilitas kesehatan tempat penelitian, orang tua/wali peserta penelitian akan mendapatkan konsumsi selama kegiatan penelitian berlangsung. Setiap peserta akan mendapatkan jaminan asuransi selama mengikuti penelitian (termasuk biaya perawatan, obat-obatan), sesuai dengan ketentuan asuransi.Peserta akan mendapatkan sertifikat keikutsertaan bingkisan dan kenang-kenangan setelah menyelesaikan seluruh prosedur penelitian. |
| Perlindungan |
| Keikutsertaan anak Anda dalam penelitian ini bersifat sukarela (tidak ada paksaan)Pada keadaan tertentu, peserta dapat menghentikan keikutsertaan dalam penelitian ini tanpa diberikan sanksi.Peneliti dapat menghentikan keikutsertaan peserta dari penelitian ini untuk kepentingan dan keselamatan peserta.Selama berlangsungnya penelitian, peserta akan mendapat pemantauan kesehatan melalui catatan yang tersedia, pengambilan darah, dan juga memungkinkan untuk dilakukan pemeriksaan lainnyaSelama berlangsungnya penelitian, peserta dapat berkonsultasi dengan dokter peneliti.Selama berlangsungnya penelitian, bila terdapat efek samping atau Kejadian Tidak Diinginkan maka akan diberi pertolongan dan dibebaskan dari biaya yang diperlukan sesuai dengan ketentuan asuransi. Peserta akan diberikan surat persetujuan dan lembar informasi untuk mengikuti penelitian, setelah mendapat penjelasan seluruh seluk beluk penelitian, kemungkinan risiko dan kewajiban-kewajibannya. |
| Kontak yang Dapat Dihubungi |
| Selama berlangsungnya penelitian ini peserta dapat berkonsultasi dengan dokter/peneliti. Apabila ada hal-hal yang tidak diinginkan peserta dapat langsung menghubungi nomor (dapat dihubungi 24 jam) atau hubungi tim peneliti berikut: |
| No | Nama RS, Kota/Kab, Provinsi | Ketua Peneliti | Nomer HP Hotline |
| 1 | RSUD Dr. H. Abdul Moeloek, Bandar Lampung, Lampung | dr. Prambudi Rukmono, Sp.A(K) | 08522-5100023 |
| 2 | RSUD Hj. Anna Lasmanah, Banjarnegara, Jawa Tengah | dr. Dyah Perwitasari, M.Sc., Sp.A | 08522-5100038 |
| 3 | RS Universitas Udayana, Badung, Bali | dr. Komang Ayu Witarini, Sp.A(K) | 08522-6047714 |
| 4 | RSUD Bali Mandara, Denpasar, Bali | dr. Ida Ayu Sri Kusuma Dewi, M.Sc., Sp.A | 08522-6057963 |
| 5 | RS Universitas Mataram, Mataram, Nusa Tenggara Barat | dr. Putu Aditya Wiguna M.Sc Sp.A | 08522-5100053 |